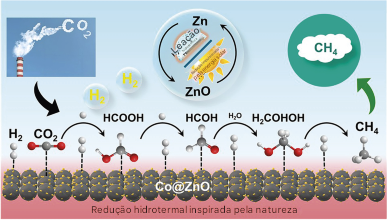
A equipe da Universidade Jiao Tong de Xangai desenvolveu um catalisador com estrutura de favo de mel, feito de metais comuns, que transforma 100% do CO2 em metano, um combustível valioso que pode ser armazenado e transportado por gasodutos existentes. Essa abordagem hidrotérmica combina energia solar com fontes subterrâneas de calor, oferecendo um caminho sustentável para converter gases de efeito estufa em energia útil, ao mesmo tempo em que potencialmente fecha o ciclo do carbono.
Imitando a química natural da Terra
A inspiração para este trabalho veio do estudo de como a natureza produz hidrocarbonetos no subsolo. Em fontes hidrotermais submarinas e no manto terrestre, substâncias químicas simples reagem com água quente e metais comuns para criar compostos orgânicos — um processo que pode ter contribuído para a origem da vida.
A equipe de pesquisa, liderada pelos professores Daoping He e Fangming Jin, projetou seu sistema para replicar essas condições naturais. Eles usam zinco como redutor e cobalto como catalisador em água quente pressurizada, criando condições semelhantes às encontradas em sistemas hidrotermais de águas profundas, onde moléculas orgânicas se formam espontaneamente.
Diferentemente dos métodos convencionais de conversão de CO2, que exigem gás hidrogênio puro ou catalisadores caros de metais nobres, essa abordagem gera seu próprio hidrogênio por meio da oxidação de zinco, usando materiais abundantes e baratos.
Um catalisador automontável
O que torna este sistema particularmente elegante é a forma como o catalisador se forma durante a reação. Quando o zinco e o cobalto reagem em água quente, o zinco oxida, criando nanofolhas de óxido de zinco que crescem diretamente na superfície do cobalto em um padrão de favo de mel.
Essa estrutura automontada, denominada Co@ZnO, resolve um grande problema que afeta os catalisadores de cobalto há décadas: eles normalmente são contaminados por oxigênio e vapor d’água, perdendo sua atividade. O revestimento de óxido de zinco atua como um escudo protetor, ao mesmo tempo que aprimora as propriedades catalíticas do cobalto.
Os pesquisadores utilizaram técnicas avançadas de raios X para examinar o interior da estrutura do catalisador, revelando que o óxido de zinco não se limita a revestir o cobalto, mas também cria um ambiente eletrônico especial que faz com que o CO2 adira com mais força à superfície do catalisador. Essa ligação aprimorada é crucial para uma conversão eficiente.
Principais Conquistas Técnicas:

Caracterizações do catalisador Co@ZnO. a XRD, b , c Imagens SEM, d – g Análise SEM–EDS. h Imagens HRTEM, IFFT, transformada rápida de Fourier inversa
☆ 100% de conversão de CO2 em metano em condições otimizadas
☆ Sem subprodutos indesejados como monóxido de carbono ou hidrocarbonetos superiores
☆ O catalisador permanece estável em vários ciclos de reação
☆ Utiliza apenas metais não preciosos abundantes na terra
☆ Formação de nanoestrutura de favo de mel automontável
☆ Resolvendo o problema de estabilidade do cobalto
O cobalto é há muito reconhecido como um excelente catalisador para a conversão de CO₂ em metano, mas sua tendência a oxidar e desativar em condições úmidas tem aplicações práticas limitadas. A equipe de Xangai resolveu esse problema por meio de uma engenharia cuidadosa do ambiente de reação.
O zinco em seu sistema cria uma atmosfera fortemente redutora que mantém o cobalto em seu estado metálico ativo. Ainda mais inteligente, o revestimento de óxido de zinco atua como um “reservatório de hidrogênio” que pode dividir moléculas de hidrogênio e alimentar átomos de hidrogênio diretamente na superfície do cobalto quando necessário.
Usando experimentos especializados de redução programada por temperatura, os pesquisadores mostraram que seu catalisador Co@ZnO poderia ser reativado em temperaturas muito mais baixas do que os catalisadores de cobalto convencionais — evidência de que o revestimento de óxido de zinco fornece regeneração contínua.
Seguindo a trilha do ácido fórmico
Para entender exatamente como o CO2 se transforma em metano, a equipe utilizou espectroscopia infravermelha em tempo real para observar as mudanças nas moléculas durante a reação. Isso revelou um detalhe crucial frequentemente ignorado em estudos sobre catalisadores: o caminho da reação é tão importante quanto o resultado final.
A pesquisa mostrou que o CO2 primeiro se converte em ácido fórmico, que então se transforma em formaldeído antes de finalmente se transformar em metano. Importante ressaltar que a reação evita completamente a formação de monóxido de carbono — um subproduto indesejado comum que pode envenenar catalisadores e reduzir a seletividade.
Essa seletividade da via explica por que a equipe alcançou 100% de conversão sem produzir a mistura de produtos tipicamente observada em reações de metanação de CO2. O revestimento de óxido de zinco parece guiar a reação ao longo da rota do ácido fórmico, enquanto bloqueia a formação de monóxido de carbono.
Economia energética parece promissora

a 5 min, b 10 min, c 30 min, d 1 h (condições de reação: 280 °C, 60 mmol Zn, 40 mmol Co, 1,5 MPa CO 2 , 0,1 mol/L NaOH, 280 °C foi selecionado deliberadamente para retardar o crescimento do catalisador Co@ZnO)
Um grande obstáculo para qualquer processo industrial de conversão de CO2 é a eficiência energética. Os pesquisadores de Xangai calcularam o balanço energético do seu sistema e encontraram resultados encorajadores que não eram enfatizados em reportagens típicas.
A análise deles mostra que, após o processamento de apenas três mols de CO2, a energia liberada pela reação excede a energia necessária para aquecer os materiais de partida. Acima desse ponto de equilíbrio, o processo se torna positivo em termos de energia líquida — um fator crucial para a viabilidade comercial.
Esta análise energética sugere que o processo pode ser economicamente sustentável, especialmente quando combinado com fontes de energia renováveis ou calor residual de processos industriais.
Integração Solar e Inspiração Geológica
Os pesquisadores imaginam que seu sistema operará como parte de uma abordagem híbrida solar-geológica. A energia solar regeneraria o zinco metálico a partir do óxido de zinco acima do solo, enquanto a conversão de CO2 ocorre em ambientes hidrotermais subterrâneos que fornecem calor e pressão naturais.
Essa abordagem biomimética se inspira em como a atmosfera primitiva da Terra pode ter sido transformada por reações semelhantes de metal-água-CO2 que ocorreram em sistemas hidrotermais bilhões de anos atrás.
Metano como combustível de ponte
Embora o metano seja, em si, um gás de efeito estufa, os pesquisadores argumentam que o metano sintético a partir do CO2 poderia servir como combustível neutro em carbono, já que o carbono originalmente veio da atmosfera. O metano pode ser armazenado indefinidamente e transportado pela infraestrutura de gás natural existente.
Mais importante ainda, essa abordagem poderia ajudar a equilibrar as redes de energia renovável convertendo o excesso de energia solar ou eólica em combustível químico armazenável durante os períodos de pico de produção.
Comparando catalisadores
A equipe de pesquisa testou seu catalisador Co@ZnO em comparação com outros catalisadores comuns de metanação, incluindo níquel, ferro, cobre e até mesmo os caros platina e paládio. Nenhuma das alternativas atingiu mais de 30% de conversão de CO2 nas mesmas condições, destacando as propriedades únicas de sua combinação de óxido de cobalto e zinco.
Mesmo ao usar gás hidrogênio puro em vez de hidrogênio gerado por zinco, o catalisador Co@ZnO superou os catalisadores de cobalto convencionais ao manter maior seletividade para metano em relação a produtos indesejados, como monóxido de carbono e ácido acético.
Estabilidade através de múltiplos ciclos

Caracterizações do catalisador Co@ZnO e Co. comercial a Espectros XPS de Co@ZnO e Co. comercial pré-reduzido b Análise de H 2 -TPR de Co@ZnO e Co. comercial expostos ao ar
Catalisadores industriais devem manter a atividade por meio do uso repetido, e o sistema Co@ZnO demonstrou durabilidade impressionante. Os pesquisadores realizaram a reação cinco vezes consecutivas e estenderam reações individuais para 10 horas sem observar degradação do catalisador.
A análise após esses testes prolongados mostrou que a estrutura do óxido de zinco em forma de favo de mel permaneceu intacta, e apenas traços de cobalto foram lixiviados na solução de reação — níveis muito abaixo dos que indicariam a quebra do catalisador.
Os desafios técnicos permanecem
Apesar dos resultados promissores, vários desafios de engenharia precisam ser enfrentados antes que essa tecnologia alcance escala industrial. A reação requer altas temperaturas (250-325 °C) e pressões (1,5 MPa), exigindo projetos de reatores robustos e gerenciamento cuidadoso do calor.
As condições alcalinas necessárias para a dissolução ideal de CO2 também podem representar problemas de compatibilidade de materiais em sistemas de larga escala. Os pesquisadores descobriram que manter o equilíbrio correto do pH é crucial para atingir o rendimento máximo de metano.
Olhando além do laboratório

Medição XAFS síncrotron e desempenho catalítico do catalisador Co@ZnO. a Espectros XANES de borda K de Co do catalisador Co@ZnO e amostras de referência, b Função χ( k ) ponderada por k3 transformada de Fourier (FT) dos espectros EXAFS para a borda K de Co, c Curvas de ajuste EXAFS correspondentes no espaço R, d WTs correspondentes para os sinais EXAFS de borda K de Mn ponderados por K3 de Co@ZnO, folha de Co e CoO, e TPD de CO2 do catalisador Co@ZnO e Co comercial pré-reduzido, f Cálculos DFT comparativos do catalisador Co@ZnO e Co comercial pré-reduzido
A equipe já está explorando como ampliar seu processo e integrá-lo a sistemas de energia renovável. Eles estão particularmente interessados em acoplar seu conversor de CO₂ a sistemas solares térmicos que possam fornecer tanto a energia de regeneração do zinco quanto o calor da reação.
O trabalho futuro se concentrará no desenvolvimento de projetos de reatores mais eficientes e na exploração de se outros metais abundantes na Terra poderiam substituir o zinco ou o cobalto, mantendo a alta eficiência de conversão.
Implicações para o ciclo do carbono

Estudo de FTIR in situ e mecanismo proposto. a Espectros de FTIR hidrotérmico in situ de metanação de CO 2 com Zn e Co, b perfil de energia de reação de HCOOH como intermediário, c ilustração esquemática do mecanismo de reação propost
Se for escalonada com sucesso, essa tecnologia poderá contribuir para o fechamento de ciclos artificiais de carbono, nos quais o CO2 capturado de emissões industriais ou diretamente do ar é convertido novamente em combustíveis úteis. O metano produzido poderá substituir o gás natural fóssil em aquecimento, geração de energia ou fabricação de produtos químicos.
Os pesquisadores enfatizam que sua abordagem oferece um “processo direto de uma etapa para conversão altamente eficiente de CO2 e síntese de catalisadores”, simplificando potencialmente a implementação industrial em comparação aos processos de várias etapas que exigem catalisadores pré-fabricados.
A concretização desse sucesso laboratorial na indústria dependerá de fatores econômicos, incluindo o custo da energia renovável, as políticas de precificação do carbono e as melhorias contínuas na durabilidade do catalisador e no projeto do reator. Mas, por enquanto, a obtenção de 100% de conversão de CO2 usando metais comuns representa um passo significativo para tornar a fotossíntese artificial economicamente viável.